?肝脏细胞凋亡增加是包括病毒性肝炎、胆汁阻塞、肝脏移植和药物引发的肝损伤等多种肝脏疾病的典型特征,深入了解肝细胞凋亡的发生过程有助于开发治疗肝脏相关疾病的新靶点,但目前人们对于肝细胞凋亡和肝损伤发生过程的认识还比较有限。
2021年12月2日,广州医科大学附属肿瘤医院张笑人团队在国际知名期刊CellDeath and Differentiation(IF:15.828)在线发表了题为“Bcl-3promotes TNF-induced hepatocyte apoptosis by regulating thedeubiquitination ofRIP1”的研究成果。该研究发现非典型IκB家族成员Bcl-3通过抑制TNF激活的RIPK1分子的泛素化修饰,促进凋亡复合体形成,最终促进TNF诱导的肝(癌)细胞凋亡。该项研究为TNF引起的急性肝损伤和肝癌提供了新的治疗靶点。

急性肝损伤能够在短时间内造成肝细胞大量凋亡坏死,致使器官丧失功能,在临床上具有极高致死率。目前唯一有效的治疗方法只有肝脏移植,而供体肝来源短缺、配型成功率低以及术后恢复困难等因素严重阻碍了该病的治疗。已有研究显示,TNF诱导肝细胞凋亡是急性肝损伤发生的主要因素之一,但具体机制尚未明晰。

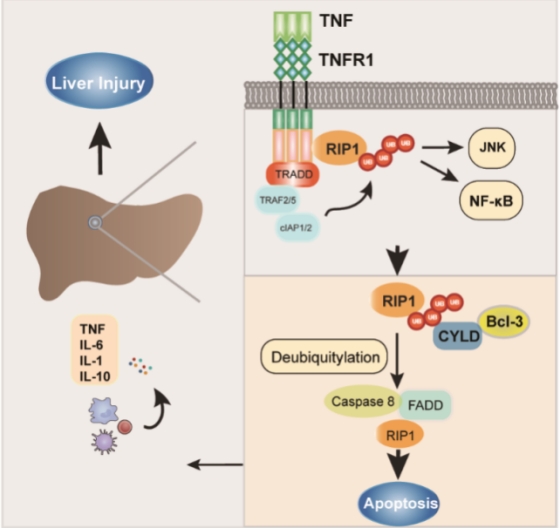
我院研究团队通过构建TNF特异性诱导急性肝损伤的动物模型,发现Bcl-3参与调控TNF诱导的肝细胞凋亡及肝损伤,敲除Bcl-3显著抑制了TNF引起的肝毒性作用。同时也发现Bcl-3促进TNF诱导的肝癌细胞凋亡。通过深入研究Bcl-3的调控机制,研究团队发现Bcl-3能够通过直接与去泛素化酶CYLD相互作用抑制RIPK1的泛素化修饰,进而促进TNF-TNFR1下游凋亡复合体的形成,促进正常肝细胞或肝癌细胞凋亡;此外,凋亡的肝细胞增多能够通过招募炎性因子浸润,进而加重小鼠的肝损伤程度。
广州医科大学附属肿瘤医院胡一鸣博士和张浩浩博士为本文的共同第一作者,张笑人教授为本文的通讯作者。